Serce z komórek raka — symbol, który prowokuje naukę
Zdjęcie komórek raka piersi ułożonych w kształt serca, wykonane przez pacjentkę i badaczkę podczas terapii, obiegło światowe media. Stało się nie tylko poruszającym symbolem, ale również punktem wyjścia do ważnej rozmowy: o tym, że choroba nowotworowa to nie tylko zbiór pojedynczych zmutowanych komórek, ale złożona, dynamiczna architektura tkanek.
Nowoczesna onkologia coraz częściej odchodzi od patrzenia na komórki w izolacji. Coraz większe znaczenie zyskuje przestrzenna organizacja guza — to, jak komórki nowotworowe układają się względem siebie, względem naczyń, tkanki podporowej (stroma) i komórek układu odpornościowego.
To właśnie ta mikroarchitektura, niewidoczna w medialnych obrazach, może decydować o agresywności nowotworu i odpowiedzi na leczenie.
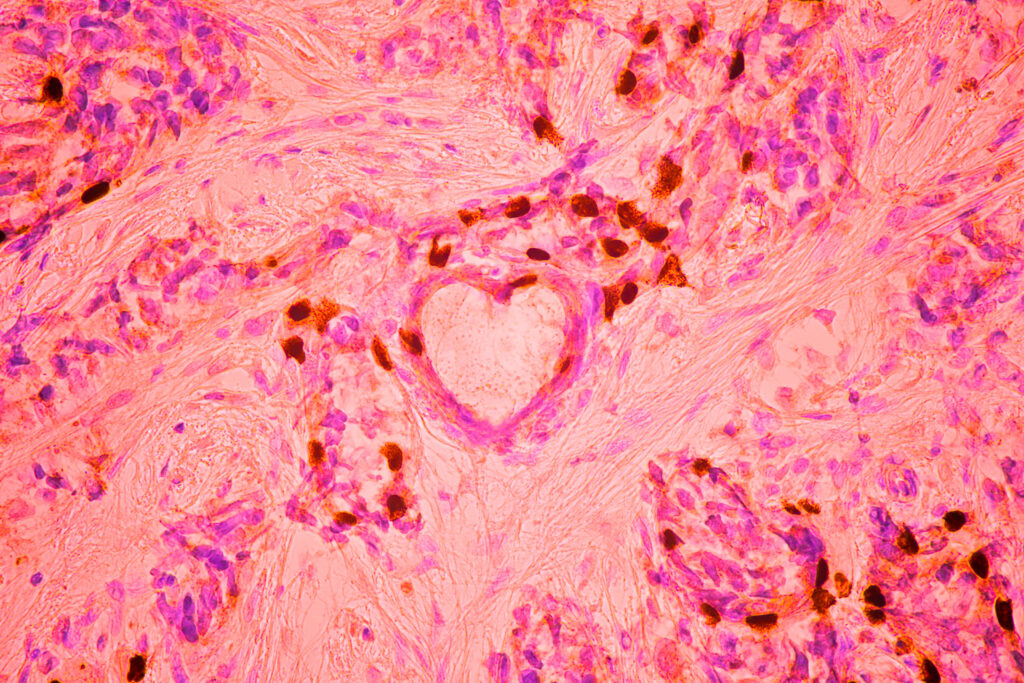
Architektura przestrzenna guza — ukryty wymiar raka
Tradycyjna histopatologia skupiała się na cechach pojedynczych komórek: wielkości jąder, liczbie mitoz, stosunku jądrowo-cytoplazmatycznym. Najnowsze badania pokazują, że równie istotne jest to, jak komórki są rozmieszczone i jak współdziałają z otoczeniem.
- W analizach przestrzennych guzów potrójnie ujemnego raka piersi (TNBC) zidentyfikowano powtarzalne „sąsiedztwa komórkowe” — klastry nowotworowych, odpornościowych i śródbłonkowych komórek, które współistnieją w określonych wzorcach. Niektóre z tych wzorców korelowały z gorszym rokowaniem i opornością na chemioterapię.
- Inne badania pokazały, że organizacja włókien macierzy zewnątrzkomórkowej (ECM) steruje ruchem i inwazyjnością komórek nowotworowych, tworząc „ścieżki” migracji wewnątrz guza.
- Analizy grafowe (cell-graphs) całych preparatów histologicznych wskazują, że gęstość połączeń między komórkami nowotworowymi i stroma jest predyktorem nawrotów i przerzutów.
Te odkrycia przesuwają punkt ciężkości z genetyki na morfologię i organizację przestrzenną — coś, co do niedawna było traktowane jako „tło”, a teraz staje się nowym biomarkerem.
TNBC — heterogeniczność, stroma i mikrośrodowisko guza
Potrójnie ujemny rak piersi to szczególnie dobry przykład, bo jest skrajnie heterogenny. Nie tylko różni pacjenci mają różne mutacje, ale nawet w obrębie jednego guza występują odmienne populacje komórek i mikrośrodowisk.
- W niektórych regionach dominują zwarte klastry komórek nowotworowych otoczone fibroblastami i kolagenem, tworzące barierę mechaniczną dla leków.
- W innych pojawiają się strefy bogate w naczynia i komórki odpornościowe, które sprzyjają inwazji i przerzutom.
- Obecność lokalnych gradientów hipoksji (niedotlenienia) w obrębie guza powoduje aktywację genów oporności na leczenie i wzrost agresywności komórek.
Te mikrośrodowiska nie są przypadkowe — mają strukturę, która wpływa na przebieg choroby. Ich analiza wymaga nowoczesnych metod obrazowania: spatial transcriptomics, profilowania białek w kontekście tkankowym i sztucznej inteligencji do analizy obrazów całych preparatów histopatologicznych.
Co może wynikać z „sercowego” obrazu
W tym kontekście fotografia komórek raka ułożonych w kształt serca może pełnić rolę symbolicznego teasera — przypominać, że układ komórek nie jest tylko estetyką, ale może być nośnikiem informacji biologicznej.
W przyszłości możliwe jest:
- tworzenie atlasów przestrzennych guzów piersi i innych nowotworów,
- identyfikowanie „układów wysokiego ryzyka” na podstawie architektury,
- dostosowanie terapii do konkretnego mikrośrodowiska w obrębie guza,
- włączanie analizy przestrzennej do rutynowych raportów histopatologicznych.
Takie podejście mogłoby całkowicie zmienić sposób, w jaki interpretujemy obrazy histologiczne — z estetycznych fotografii w mapy funkcjonalne guza.
Podsumowanie
Fotografia komórek raka w kształcie serca porusza emocje, ale jej największa wartość może leżeć w tym, że prowokuje pytania. Współczesna onkologia zmierza w stronę analizowania nie tylko tego, z czego zbudowany jest guz, ale również jak jest zorganizowany.
Być może przyszłość diagnostyki onkologicznej leży właśnie w tym ukrytym wymiarze — w strukturze, topologii i przestrzennej logice nowotworu.
Bibliografia
- Pati P., Jaume G., Fernandes L.A. et al. HACT-Net: A Hierarchical Cell-to-Tissue Graph Neural Network for Histopathological Image Classification. npj Digital Medicine, 2024.
- Wu X., Liu Y., Wang T. et al. Spatial Architecture of Tumor Microenvironment in Triple Negative Breast Cancer Predicts Therapy Response. Modern Pathology, 2024.
- Garcia-Ruiz S., Martin-Perez D. et al. Self-organisation of invasive breast cancer driven by the interplay of active and passive nematic dynamics. Nature Physics, 2024.
- Curtis C. et al. The genomic and transcriptomic architecture of breast cancer subtypes. Cell Reports, 2023.
- Lyon A.R., López-Fernández T., Couch L.S. et al. 2022 ESC Guidelines on cardio-oncology. European Heart Journal, 2022.
Źródła obrazu i link do fotografii
Galeria Nikon Small World 2023 — Breast Cancer Cells: https://www.nikonsmallworld.com/galleries/2023-photomicrography-competition/breast-cancer-cells Nikon Small World
Przeczytaj również:
